女性肾移植受者的妊娠与生育问题

一、妊娠与生育的特点、时机和条件
(一)妊娠的特点
通常女性每月产生一个卵子,女性可以缺乏性欲或不具有健全的性功能,但可妊娠、生育。育龄女性绝经期(更年期)有月经停止,标志生育能力的终止。但尿毒症可导致患者全身多个系统以及多个器官的损害,尿毒症可引起患者性功能,性激素、以及生育能力的改变。女性尿毒症患者常出现下丘脑-垂体-性腺轴功能紊乱,伴有卵巢功能低下、月经紊乱而导致生育能力下降或因停经而导致不孕。而成功的肾移植后,受者内分泌及生殖系统功能可随移植肾功能的恢复,月经和排卵功能也逐渐恢复,大多数移植后不久恢复了生殖功能。但很多女性受者往往不了解这一生理特点,而认为肾移植术后月经未恢复或性生活少就不会发生妊娠,因而未采取有效的避孕措施,导致非意愿妊娠的发生。
由于移植不久后的计划外妊娠将给母亲和胎儿带来难以想象的危险,由于先兆子痫、早产、低出生体重概率上升及剖宫产风险的增加,所以建议这些妇女应接受避孕咨询。建议短期内避孕采取避孕套或口服避孕药;由于肾移植可提高生育力,因此对于不愿意生育的受者应该采取有效的避孕措施;无生育要求者可在移植手术的同时行输卵管结扎术。由于男性在决定和使用有效的避孕方法方面有着十分重要的作用,因此促进男性积极参与避孕活动和与女性的合作,切实落实节育措施,只有这样才能防止和减少肾移植受者非意愿妊娠的发生。
(二)生育的时机
肾移植后的育龄妇女随着肾功能的恢复,月经和排卵功能逐渐恢复,较容易妊娠,但是女性生育的最大争议问题是免疫抑制剂是否对胎儿的影响,而女性尚有孕育胎儿过程中增大的子宫对移植肾的压迫、血流动力学的改变等高风险因素的影响。因此女性肾移植受者术后何时能妊娠、生育目前还没有一个明确的定论。但文献报道受者生育一般在肾移植术后肾功能正常状态的第3~4年为最多,Stratta等主张在肾移植术后2~5年妊娠。过早妊娠会加重肾脏损害,出现排斥,妊娠不易成功,且对妊娠妇女有一定的危险。但是随着各种新的免疫抑制剂的应用,术后排斥发生率明显减少,因此也有学者认为移植1年后移植物稳定,可以妊娠生育。2005年NTPR认为如果有稳定的免疫抑制剂用量和足够的肾功能水平作为先决条件,则移植后妊娠的最短时间应是1年。
(三)生育的条件
1.美国移植界妇女健康委员会认为有关女性生育条件:
(1)移植受者在过去的一年无排异反应。
(2)足够稳定的移植肾功能(肌酐小于1.5mg/L,GFR未定)无或者微量蛋白尿。
(3)无可能影响胎儿的急性感染。
(4)保持稳定的免疫抑制剂用量。
2.结合文献,我们认为女性受者术后妊娠、生育比较适合的时机与条件应为:
(1)成功的肾移植手术2年后,身体条件适合产科要求。
(2)Pred 5~10mg/d、Aza 50mg /d、Cs剂量在3mg/(kg·d)以下,如正在使用霉酚酸制品而要求生育者,必须停用吗替麦考酚酯制品至少6周后,才可以受孕。
(3)年龄在35周岁以下。
(4)全身状况良好,无排斥反应发生。
(5)肝、肾功能状态正常。
(6)无高血压或轻度高血压(血压≤140/90mmHg),且药物能控制。
(7)无血尿、蛋白尿或微量血尿、蛋白尿(蛋白尿小于500mg/24h)。
(8)B超检查移植肾无排异迹象,无积水,无结石,无输尿管扩张。
(9)此外,在妊娠后需进一步加强产前检查,以确保优生优育。
二、分娩方式的选择与终止妊娠的指征
(一)分娩方式的选择
移植肾位于髂窝内,并不阻碍产道,不会造成产道梗阻和机械性损伤,若无产科原因,可自然分娩。但是由于肾移植受者术前长期肾衰竭或长期透析,或长期使用皮质激素所造成的骨盆骨营养不良;妊娠过程中增大的子宫对移植肾有时可产生压迫,容易出现肾功能损害;妊娠容易出现严重的妊高征,胎儿宫内状况不良等原因,是剖宫产的比例增高。Ghafari A等报道了53例移植受者的61次妊娠,其中24次剖宫产(45.2%)。国内于立新等报道13例成功妊娠分娩,全部选择了剖宫产(100%),我们报道25例肾移植受者妊娠中23例剖宫产(92%)。国内剖宫产高的主要原因是:社会因素:如珍贵儿,年龄>30岁,产妇及家属要求剖宫产;妊娠高血压;移植肾受压或肾功能损害者等。其实肾移植术后分娩方式的选择主要是取决于产科的情况,如无产科剖宫产的指征,推荐进行阴道分娩。
如出现以下情况时可以考虑进行剖宫产:
1.长期肾衰竭或长期透析,或长期使用皮质激素所造成的骨盆骨营养不良者。
2.产道狭窄、畸形等。
3.中、重度妊高征、胎儿宫内窘迫、脐带绕颈者。
4.移植肾受压者或移植器官功能损害并逐渐加重等。
(二)终止妊娠的指征
为保证母体及移植器官的安全,有下列指征者必须终止妊娠:
1.产科原因如重度妊高征、胎儿宫内窘迫、胎膜早破、胎儿畸形、胎死宫内者。
2.发生排斥反应,肾功能严重损害并逐渐加重,危及移植肾存活者。
3.持续有尿蛋白或尿蛋白加重者。
4.泌尿生殖系统严重疾病等。
三、免疫抑制剂对胎儿的影响
肾移植受者术后需长期应用免疫抑制剂,由于免疫抑制剂可以通过胎盘达到胎儿体内,对胎儿可能造成影响,因此制定合理的免疫抑制治疗方案,既要保护受者及移植肾功能的健康存活,又要保证妊娠成功及胎儿正常生长发育。但免疫抑制剂对人类生殖系统的毒性机制还不十分清楚,目前仅对几种免疫抑制剂进行了实验研究。美国食品和药品管理局(FDA)根据免疫抑制剂对生育的影响可分为:
A类:对人类无风险证据的。
B类:动物实验显示有危险性,但无人类危险性的证据,如皮质激素类(泼尼松、泼尼松龙、地塞米松、甲泼尼龙)等。
C类:不可排除风险的,如Cs、Tac等。
D类:有风险证据的,如硫唑嘌呤、霉酚酸制剂。
X类:禁忌使用的。
(一)皮质激素
动物试验表明,母体服用大剂量皮质类固醇可能引起胎儿畸形。皮质类固醇激素在小鼠和兔的实验中有致畸作用,但在大鼠中未观察到此现象。皮质激素使胎膜结缔组织薄弱,妊娠中晚期易发生胎膜早破,从而诱发流产或早产。糖皮质激素可通过胎盘,可增加胚胎腭裂、胎盘功能不全、自发性流产、胎儿宫内发育迟缓、死胎、新生儿肾上腺皮质功能减退的发生率。因未作过足够的人类生殖研究,因而当皮质类固醇用于妊娠妇女、哺乳妇女或可能妊娠的妇女时,应仔细衡量它的益处与它对母亲和胚胎或胎儿潜在危险之间的关系。
有报道,泼尼松与某些偶发的出生缺陷有关,当其剂量超过20mg/d时更易出现。可的松、泼尼松和地塞米松容易通过胎盘,但90%在到达胎儿以前已在胎盘中被代谢。甲泼尼龙能在胎盘中充分代谢,胎儿血循环中仅能检出少量。皮质激素在胎盘中的充分代谢可以保护胎儿免受药物的不良影响。
(二)环孢素(CsA)
CsA属钙调磷酸酶抑制剂(CNI),很容易通过胎盘进入胎儿血循环。CsA在羊水、胎盘和胎儿组织中均能检出,胎盘和脐带血中的药物浓度比母体血循环中的浓度还高。但CNI在胎儿血液中的浓度仅是母体的一半,这可能和胎儿肝脏代谢有关。也有研究发现,新生儿血清和母体血清一样,对培养的T淋巴细胞具有同等程度的免疫抑制作用。
2013年8月,CsA药品说明修改中指出:标准试验(大鼠每日口服给药至17mg/kg和家兔每日口服给药至30mg/kg)表明CsA没有致突变或致畸作用。CsA在产生毒性的剂量下(大鼠每日口服给药30mg/kg和家兔每日口服给药100mg/kg)具有胚胎和胎儿毒性,表现为产前和产后死亡率增加,胎儿体重下降并同时伴有相应的骨骼发育迟缓。但CsA对人类生育力影响的数据有限。
妊娠期服用CsA的受者所生子女中23.9%(17/71)学龄儿童出现发育迟缓,Cruz等也报道一组60例受者75次妊娠中有12名发育迟缓。我们报道25例肾移植受者在妊娠期间有23例服用CsA,其剂量在1.2~3mg/(kg·d),在所生的子女中未发现新生儿发育迟缓,是否与国内受者服用CsA的剂量低有关?有必要对这些子女进行长期随访和进行前瞻性研究。
(三)他可莫司(Tac)
Tac和CsA均属钙调磷酸酶抑制剂(CNI),很容易通过胎盘进入胎儿血循环。2011年11月Tac产品说明修改中指出:在大鼠和兔的实验中,Tac在母体毒性剂量下可导致小鼠胚胎毒性及胚胎发育迟缓,Tac可影响雄性大鼠的生殖能力。Tac与其他免疫抑制药物相比,并未增加妊娠过程和结局不良反应,到目前为止,还没有其他相关流行病学资料。妊娠妇女因治疗需要,如果没有其他更安全的疗法并且只有在受者潜在的益处大于对胎儿的潜在风险,才可以使用本品,如果在子宫内有药物暴露,建议监测Tac对新生儿潜在的不良反应。
各种器官移植受者,应用CsA作为基础免疫抑制剂者妊娠后的活产率高于使用Tac者。但有资料显示,使用Tac的产科及产后情况同正常人群相似,其Tac的应用剂量较以前减少,谷浓度为5~10μg/L。因此,Tac对胎儿的不良影响可能与剂量相关。这些胎儿发育异常与免疫抑制剂的关系,尚需进一步研究。
(四)硫唑嘌呤
硫唑嘌呤FDA分类为D类(有人类危险的直接证据)。硫唑嘌呤可以通过胎盘进入胎儿血循环,硫唑嘌呤也可造成不同种群动物后代短暂的染色体异常。有研究发现,该药在胎儿体内仅以非活性的代谢物形式存在,提示胎儿缺乏次黄嘌呤磷酸化酶,该酶可以将硫唑嘌呤转化成其活性形式6-巯基嘌呤。由于硫唑嘌呤可引起啮齿类动物骨骼肌、内脏及血液学异常,以及人类胎儿免疫抑制和结构畸形,因此应建议接受本品治疗的受者的配偶需采取充分的避孕措施。如果受者妊娠,则需慎重权衡利弊。妊娠妇女服用硫唑嘌呤后,在胎儿血液和羊水中均可测到低浓度的硫唑嘌呤或其代谢产物。有报道称曾有部分在妊娠期服用过硫唑嘌呤的妊娠妇女所产下的新生儿有白细胞减少和或血小板减少症发生,故建议妊娠期用药受者额外进行血液学监测。
硫唑嘌呤和吗替麦考酚酯(霉酚酸酯)制品对人类都存在潜在的致畸作用,理论上对胎儿可能存在影响,但与其他D类免疫抑制剂比较,临床上应用硫唑嘌呤的时间最长,经验最多,因此国外经验:器官移植后要求妊娠与生育者,建议在停用吗替麦考酚酯制品转换成硫唑嘌呤6周后,才可以受孕。我们经验:硫唑嘌呤 50mg/d,这个剂量应该是比较安全的。
(五)霉酚酸制剂
霉酚酸制剂包括吗替麦考酚酯以及霉酚酸钠肠溶片。美国食品和药品管理局(FDA)曾经将此类药定为C类(人类危险性不排除),但自2007年10月,根据登记信息与药物上市后的相关数据显示,孕期使用霉酚酸制品带来的自然流产以及新生儿先天缺陷患病率风险升高,因此,美国食品与药物管理局将孕期使用霉酚酸的类别从C类改为D类。
2012年7月吗替麦考酚酯(MMF)产品说明书和2013年2月霉酚酸钠肠溶片说明书修改中均指出该药妊娠分类为D:在动物生殖毒理学研究中,当无母体毒性情况下,胎儿吸收和畸形的发生率升高。根据体表面积转换,雌性大鼠和雌性兔子接受的MMF剂量相当于肾移植和心脏移植受者所接受人用剂量的0.02~0.9倍。在大鼠子代中发生的畸形包括无眼、无下颌和脑积水。在兔子子代中发生的畸形包括心脏异位、肾脏异位、膈疝和脐疝。当将MMF给予妊娠妇女时,可能对胎儿造成致命性伤害。在妊娠期间使用MMF与前3个月流产风险升高、先天性畸形风险升高等相关,特别是外耳和其他面部异常(包括腭裂和唇裂)及四肢远端、心脏、食管和肾脏异常等。妊娠妇女应当避免使用本品,除非对胎儿的潜在益处大于潜在风险。
NTPR对术后女性使用霉酚酸制品的受者进行了重点分析:
1.孕期使用霉酚酸制品的生育情况
NTPR分析了152例女性受者在孕期使用霉酚酸制品,生育情况如下:78例活产,70例自然流产,3例死产以及1例治疗性流产。在活产婴儿中,14名是先天缺陷患者,患病率高达18%。Hoeltzenbein等报道了孕期服用霉酚酸57例受孕者,分娩结果:16例自然流产,12例手术终止妊娠(2例受者胎儿是先天畸形),29例活产中6名先天畸形儿(21%)。NTPR的另一份资料显示,24例女性移植受者在服用吗替麦考酚酯的治疗期间有33次妊娠,其中15次(45%)自然流产,18次成功生育,但有4名(22%)婴儿畸形。相比之下,受者孕期未使用霉酚酸制品产下婴儿患先天性缺陷疾病的概率仅在4.9%左右。
NTPR对受者健康、移植情况以及孩子的身体状况进行了长期的跟踪调查。与孕期未使用霉酚酸制品的女性受者相比,孕期使用霉酚酸制品的女性移植手术受者的胎儿存活率更低,而且新生儿患先天性疾病的概率更高。因此,孕期女性使用霉酚酸制品的风险较高,应建议在受孕前6周停用吗替麦考酚酯制品。
2.硫唑嘌呤替换霉酚酸制剂生育情况
NTPR另一项研究的主体,是在停用吗替麦考酚酯制品转换成硫唑嘌呤6周后,才受孕的女性移植受者。
硫唑嘌呤虽然也被美国食品与药物管理局定性为D类,但是药品医生处方信息及用药指南仍建议在受孕6周前以及孕期范围停用霉酚酸药物,很多医疗中心表示会在女性受者受孕6周前将药物替换成硫嘌唑呤。据统计:69例受者(71例次受孕并产下74名婴儿)将药物霉酚酸替换成硫嘌呤唑,以免受孕受到影响。其中,56例(46例肾脏移植受者,7例胰脏-肾脏移植受者,2例心脏和1例肺移植受者)在受孕6周之前将硫唑嘌呤替换吗替麦考酚酯,受者共受孕58次。分娩结果如下:51名活产婴儿(占88%),4名自然流产(占7%),2名死产(占4%)以及1名治疗性流产。2名死产胎儿死因与胎盘前置有关。婴儿出生缺陷疾病种类包括先天性马蹄内翻足2名以及尿道下裂2名。据跟踪调查显示,所有婴儿均身体健康,发育良好。一半受者在产后继续使用霉酚酸,最近一次对受者身体健康状况的跟踪调查证实,2例(4%)肾脏移植受者产后2年移植肾功能丧失(术后使用硫嘌呤唑),1例胰脏-肾脏移植手术受者在孕期丧失肾脏功能,剩下的53例移植受者表示移植器官功能良好。
根据NTPR的统计,所有肾脏移植人群2年内器官功能丧失概率在6%~8%左右。与孕期使用霉酚酸的受者不同的是,该组受者中并无发现任何高于一般移植受者的自然流产率以及新生儿先天性缺陷患病率(小耳症、唇裂以及腭裂)等现象。
四、免疫抑制剂对新生儿早产及婴儿母乳喂养的影响
(一)免疫抑制剂对新生儿早产的影响
早产是指妊娠满28周至不满37足周分娩。中国大陆正常人群生育早产儿的出生率在5%~7%左右,美国单胎早产儿的出生率在5.4%,但是女性肾移植受者术后生育,其早产的出生率明显增高。Oliveira等报道一组52例受者的52次妊娠中,20例(38.4%)发生了早产。Romero Arauz等和Sibanda N等也报道在肾移植受者生育中,50%发生了早产。Areia等报道其早产的出生率高达59.3%。NTPR统计了受者摄入CsA的410例妊娠分娩中54%发生了早产,受者摄入Tac 244例妊娠分娩中,早产的出生率也达54%。我们报道一组25例女性生育其早产的出生率达28%。但相比其他实体移植手术受者的孕期分娩情况,胰脏-肾脏联合移植手术受者早产的风险更高,受者摄入CsA早产达84%,受者摄入Tac早产达72%,这些受者应视为分娩高危人群。如此高的早产出生率可能与受者术后长期应用免疫抑制剂有关。文献报道皮质激素可使胎膜结缔组织薄弱,妊娠中晚期易发生胎膜早破,从而诱发流产或早产。此外还与肾移植受者妊娠晚期容易出现严重的妊高征,胎儿宫内状况不良以及移植肾出现肾功能损害等原因,因而不得不终止妊娠,提前剖宫产有关。
(二)免疫抑制剂对婴儿母乳喂养的影响
母乳是婴儿的最佳天然食物,母乳喂养对婴儿早期的体重、身长、运动和语言发育优于人工喂养;母乳喂养能增强儿童体质、降低某些疾病的发病率。但是肾移植受者需长期服用免疫抑制剂,而免疫抑制剂可能通过乳汁对婴儿造成影响。因此NTPR对许多正在使用免疫抑制药物而选择母乳喂养的女性展开了调查。
据NTPR统计有66例肾脏移植手术受者选择用母乳喂养她们的83个婴儿。而在肝脏移植手术受者组中,23例受者用母乳喂养30名婴儿。4例胰脏-肾脏移植手术受者选择用母乳喂养她们的5个婴儿。3例肺移植手术受者选择母乳喂养。6例心脏移植手术受者用母乳喂养她们的10个婴儿。1例肝脏-肾脏移植受者,术后一直服用Tac以及泼尼松免疫抑制药物,并在术后5年受孕。孕龄37周时,该例受者产下一个重达2792g的健康婴儿。在最近的跟进调查中,该例受者与婴儿的身体状况良好,受者选择母乳喂养,在母乳喂养过程中未出现任何相关问题。Gouraud等报道了14例受者中有9例选择了母乳喂养,但有3例在5~15天停用母乳喂养,并且后续没有母乳喂养。其中6名被母乳喂养的幼儿,期间受者还在使用Tac,平均每日服用Tac的剂量为9.6mg/d(4.5~15mg/d)。哺乳期的平均持续时间为3个月(1.5~6个月),婴儿随访的平均时间为8.5个月(2~30个月),所有孩子都健康成长,并没有发现任何问题或者任何感染病史,认为在服用Tac期间使用母乳喂养应该是安全的。最近的跟踪调查显示,所有被母乳喂养的孩子中并无明显问题存在。
NTPR统计在过去的18年里,母乳喂养的趋势日趋增长。因此母乳中的免疫抑制剂对子代的生长发育到底有无危害?与母乳喂养自身优点相比,哪个对子代的生长发育更加有利?尚需进一步研究。
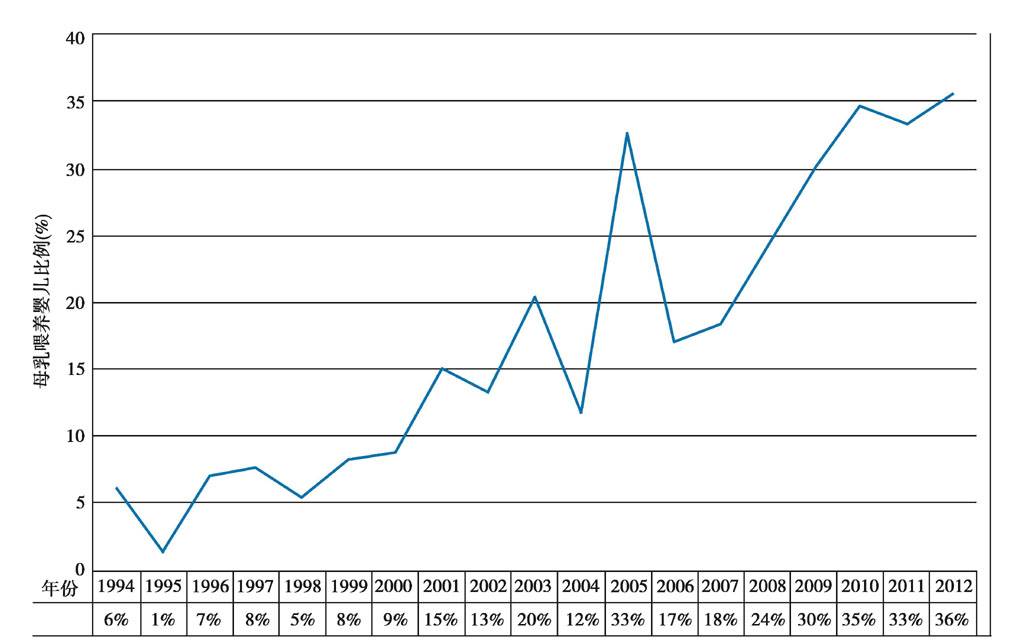
图 母乳喂养增长趋势(百分数表示接受母乳喂养的婴儿)
五、生育对移植肾及自身健康的影响
(一)妊娠与生育对移植肾的影响
女性受者妊娠与生育对移植肾有无不良影响,仍然存在争议。Kashanizadeh等回顾了1996—2002年的报道,把肾移植术后处于生育期的女性受者分为妊娠组和未妊娠组,分别追踪(45.4±22.0)个月和(46.3±19.8)个月,结果显示,两组的5年存活率无显著差异。First等研究了18例肾移植受者术后25次妊娠的资料,认为术后妊娠对移植肾功能无明显影响。
但是女性肾移植受者术后生育需要妊娠、分娩,妊娠后肾小球滤过率(glomerular filtration rate,GFR)增加,增加的幅度与GFR的基线水平有关。妊娠后GFR增加,可导致肾小球高滤过以及随之而来的肾小球硬化。Salmela等报道22例肾移植后妊娠29次的资料,移植肾10年的存活率是69%,对照组则是100%,因此认为妊娠对移植肾有不良影响。Kato等对孕期高血压与孕期器官功能丧失之间的关联性做了研究。他们将试验人员分成2组,A组平均血清肌酐含量少于1mg/dl,B组为1~2mg/dl。结果:A组受者在分娩前后所有肾功能表现比较稳定,B组部分受者在妊娠期间移植肾功能恶化。因此认为妊娠期间高血压的药物治疗对移植肾功能有显著影响,孕前高血压是影响孕期肾脏功能丧失的重要影响因素之一。即使在受者身患高血压但血清肌酐含量仍处于正常范围,还是有可能发生部分肾脏功能损失。
妊娠过程中增大的子宫对移植肾有时可产生压迫。我们曾经报告1例受者肾移植术后妊娠双胞胎,受者剖宫产前3天:移植肾彩超监测肾盂分离3.3cm,提示移植肾积水,血肌酐82μmol/L,24小时尿蛋白定量800mg。剖宫产后15天检测血肌酐79μmol/L,24小时尿蛋白定量 464mg,彩超监测移植肾肾盂分离2.0cm。产后3个月彩超复查移植肾无积水。因此若是妊娠过程中增大的子宫对移植肾产生压迫而引起的移植肾积水,分娩后可逐渐好转。
文献报道少数移植受者妊娠、分娩期间,可出现排斥反应、移植物功能不全或出现移植物功能丧失,此情况一般出现于妊娠前已有移植物功能不全者。但需注意的是:妊娠时胎盘中含有HLA-G,它是一类免疫耐受分子,所以妊娠时免疫抑制剂应用要求偏低。但是,当分娩后由于胎盘逸出,HLA-G分子迅速降低,易发生排斥。因此,分娩后要迅速增加免疫抑制剂用量,反之易致移植物排斥失功。NTPR调查发现服用CsA的受者妊娠、分娩期间发生排斥反应1%。服用Tac的受者妊娠、分娩期间发生排斥反应2%。妊娠前已有肾功能异常的肾移植受者,妊娠期间的某些危险因素如高血压、先兆子痫、感染以及剖宫产等可能导致移植肾丧失的危险性显著增加。因此妊娠前必须慎重考虑妊娠对移植物的影响。
(二)女性生育对自身健康的影响
因长期服用免疫抑制剂,肾移植受者在孕产期的高血压、先兆子痫和感染以及剖宫产的发生率明显升高。Oliveira等报道一组52例受者52次(其中两例是双胞胎)妊娠中,33例(63.5%)并发高血压;31例(59.6%)并发贫血;22例(42.3%)并发尿路感染,4例(7.7%)并发糖尿病,4例(7.7%)并发胎膜早破;20例(38.5%)发生早产。Areia A等报告28例肾移植受者的34次妊娠中,受者最常见的并发症是,18次妊娠(52.9%)并发高血压,其中有2次因先兆子痫而终止妊娠,10次妊娠(29.4%)发生泌尿系感染,3次妊娠(8.8%)发生妊娠性糖尿病,2次妊娠(5.9%)发生移植物排斥。在27例成功的妊娠分娩中,16例(59.3%)发生早产。因此认为女性妊娠在产前以及围生期存在许多问题。NTPR调查了345例服用CsA的受者共受孕528次,其中并发高血压61%,并发糖尿病12%,并发感染23%,并发先兆子痫30%,发生排斥反应1%。调查206例服用Tac的受者共受孕334次,其中并发高血压50%,并发糖尿病9%,并发感染20%,并发先兆子痫34%,发生排斥反应2%。
综上所述,女性肾移植受者术后若情况允许,可以生育,但有时可对移植肾以及自身健康带来一定影响。如果因为生育而丧失移植肾或威胁受者生命,则得不偿失。因此,对女性肾移植受者术后生育应慎重,需要进行全面评估,并应有产科、移植科以及心内科等科室的医生共同监测,以确保子女、移植肾以及受者自身的安全。


